Curso EAD – Fundamentos da Gestão de Riscos de Qualidade
21 e 22 de maio de 2020
Curso na modalidade de ensino à distância (EAD) “on line”.

Programa:
• Princípios básicos da Gestão de Riscos
• Impacto e tendências dos guias internacionais (ICH Q9 – Gestão de Riscos de Qualidade) e da legislação (Anvisa – RDC 301/2019)
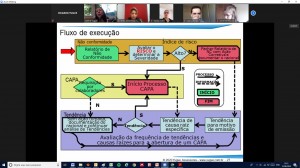
• Processo geral de Gestão de Riscos da qualidade
- Responsabilidades
- Iniciando um Processo de Gestão de Risco
- Determinação do risco
- Controle do Risco
- Comunicação do Risco
• Análise de Riscos
• Metodologias de Gestão de Riscos
• Integração de Gestão de Risco da qualidade na indústria com a área regulatória
• Aplicação de métodos e ferramentas de gestão de riscos – ICH Q9
- Métodos Básicos de Gestão de Risco
- Failure Mode Effects Analysis (FMEA) / Modo de Falha, Efeitos e Análise da Criticidade (FMECA)
- Árvore de decisão
- Análise preliminar de perigo (APP) / Preliminary Hazard Analysis (PHA)
- Análise de Perigos e Pontos Críticos de Controle (APPCC) / Hazard Analysis & Critical Control Points (HACCP)
- Estudo do Perigo e Operabilidade – Hazard and operability study (HAZOP)
• Classificação de Riscos
• Ferramentas de Apoio Estatístico
Duração total: 6 horas
Datas: 21 e 22 de maio de 2020
Horário: das 19h00 às 22h00
Ministrante: Valéria Yugue – sócia consultora da Yugue Assessores